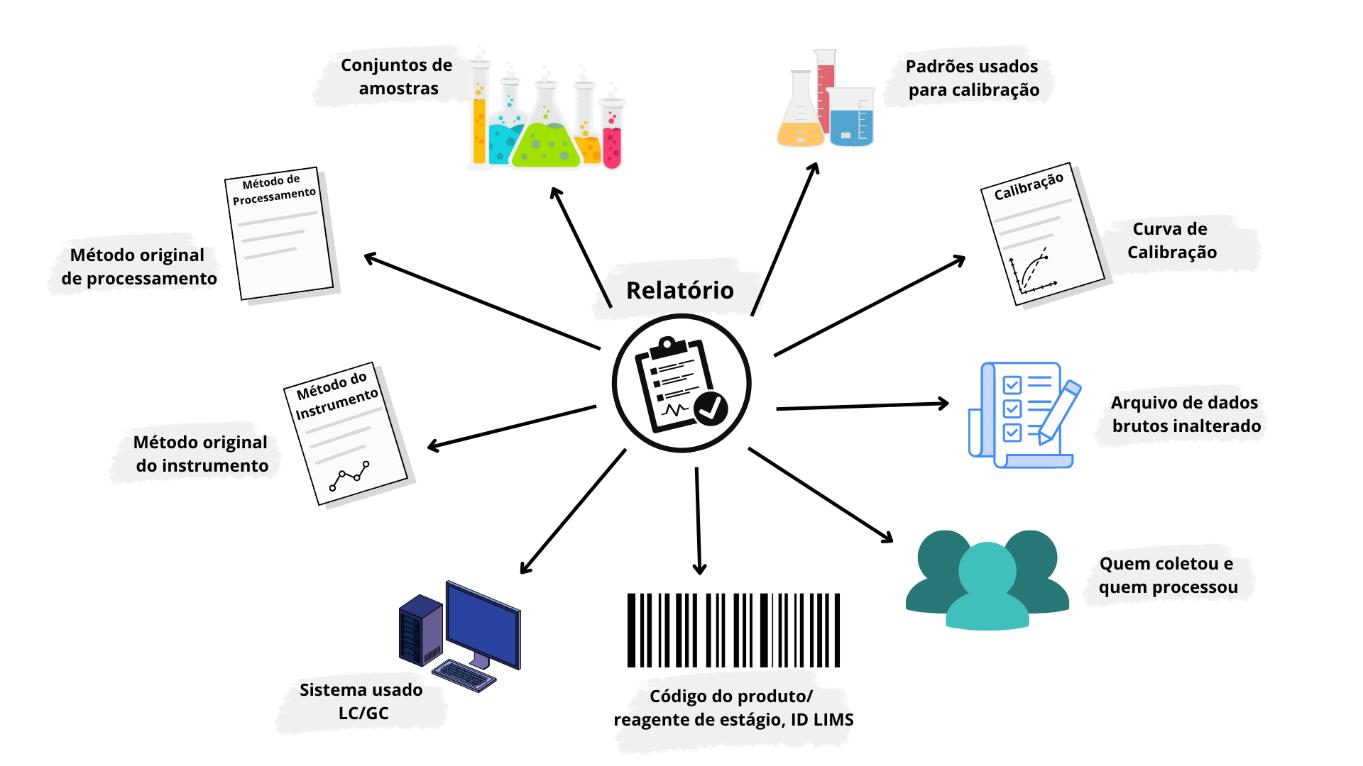
ERP é um sistema que nos desafia como profissional de VSC, a primeira reação pode ser de insegurança com um pouco de ansiedade, pois é um sistema bem complexo.
A importância do ERP para o negócio é indiscutível. Utilizado em empresas de pequeno a grande porte, responsável por todo o gerenciamento e rastreabilidade, desde a compra até a venda, permeando entre todas as áreas da empresa. É um dos principais sistemas a ser auditado. E com isso fica a pergunta: por onde começar?
Resumo aqui os passos a serem seguidos, para que a validação seja alcançada com o sucesso almejado.
1 – O primeiro passo é reunir a equipe multidisciplinar que auxiliará em toda e implementação do projeto, desde a elaboração da ERU/URS até a entrega do sistema. Pelo menos, um representante de cada área, para auxílio no entendimento das necessidades do negócio;
2 – Mapeamento do Processo – identificado os processos que serão inseridos no sistema, assim como novos processos devido a transição da atividade manual para a automatizada;
3 – Requisitos do Usuário (ERU/URS) – contemplando os requisitos, conforme demonstrado no mapeamento do processo, incluindo os requisitos regulatórios, de documentação e de infraestrutura. Esse documento deve fazer parte do contrato com o fornecedor.
4 – Seleção do fornecedor – é de extrema importância que o fornecedor tenha conhecimento no processo de ciências da vida e do setor regulado, pois há funções a serem desenvolvidas para atendimento à requisitos que são regulatórios (FDA e Anvisa). A Qualificação do Fornecedor é item obrigatório e auxilia na tomada decisão. O envio da ERU/URS ao fornecedor deve ser realizado antes da contratação, para que o mesmo possa responder o atendimento ou não ao documento. Não esquecer de colocar a ERU/URS como item do contrato que deve ser atendido em sua totalidade;
5 – Plano de Validação de Sistemas Computadorizados – descrevemos aqui a estratégia de validação, assim como os módulos que serão implementados. Nesse momento deve ser realizada a avaliação BPx de forma modular, pois nem todos os módulos tem impacto BPx, e dessa forma, não será escopo da validação.
6 – Desenvolvimento do Sistema – esse processo é de responsabilidade do implementador, porém é imprescindível que VSC e Equipe Multidisciplinar participe ativamente das reuniões e demonstrações, garantindo que os requisitos estão sendo atendidos, ou seja, que o sistema está sendo construído conforme esperado.
7-Documentação Técnica – visto que houve necessidade de parametrização/customização específica (que não é padrão/nativa do sistema), essas devem ser documentadas pelo fornecedor, descrevendo como as funcionalidades estão atendendo aos requisitos. Esse documento, geralmente nomeado de Especificação Funcional ou Descritivo Funcional ou ainda BBP (Business Blue Print), auxilia no entendimento da funcionalidade X processo e será utilizado na validação do sistema;
8 – Análise de Riscos – conforme GAMP5 2nd edition e Guia N°33/2020 os sistemas devem ser validados baseados em riscos, ou seja, nesse momento trazemos os requisitos das URS/ERU, somente dos módulos BPx relevantes (já avaliado e documentado no PV), e ainda avaliamos as funcionalidades BPx dentro de cada módulo, ou seja, nem todos os requisitos de um módulo BPx tem impacto para validação e a análise de riscos é o documento que vai demonstrar: o impacto das funcionalidades, a criticidade das funcionalidades, o atendimento das funcionalidades dentro do processo e a extensão da validação. Cabe ainda ressaltar que, riscos BPx classificados como Médio e Alto devem ser mitigados, a ação de mitigação deve ser discutida entre a equipe multidisciplinar. Riscos classificados como Baixo, podem ser assumidos pelo negócio e não necessariamente ser desafiado na validação.
9 – Qualificação do Projeto ou Revisão do Desenho (Design Review) – avaliação de forma documental se o sistema atende aos requisitos do usuário. O rigor da extensão da verificação deve ser baseado em riscos. O foco deve ser funcionalidades configuradas ou customizadas. Esse documento pode ser incorporado junto a Matriz de Rastreabilidade, conforme GAMP5 2nd.
10 – Testes em Ambiente de Testes – conforme avaliado em análise de riscos, todos os testes negativos devem ser testados nesse ambiente, somado as funcionalidades configuradas/customizadas. Essa etapa é realizada em ambiente de qualidade/homologação, para não trazer dados fictícios ao ambiente produtivo.
11 – Testes em ambiente produtivo – Essa etapa verifica a correta instalação, operação e desempenho em ambiente final, confirmando que o sistema está adequado ao processo. Importante prever a etapa de operação assistida (15 ou 30 dias), garantindo que o sistema não trouxe nenhum impacto negativo ao processo ou erros inesperados, não encontrados durante o desafio do sistema.
12 – Matriz de Rastreabilidade – documento que demonstra o atendimento do requisito do usuário aos demais documentos do ciclo de vide do sistema. Importante que esse documento comece a ser elaborado junto com a Análise de Riscos, garantindo assim, que todos os requisitos são atendidos.
12 – Relatório Final de Validação – resume todos os documentos, atividades, testes, desvios, responsáveis durante a validação do sistema. É o documento que descreve o status de validado do sistema em questão. A partir da data da emissão do RFV, inicia-se o prazo para Revisão Periódica do Sistema.